Kimyadakı Müqəddəs Grail reaksiya haqqında məlumatınız varmı?
2024,04,22
Təbii qaza gəldikdə, onunla tanış olmamalısınız və indi heç bir ev təsərrüfatını bişirə bilməz. Təbii qazın əsas komponenti ən sadə karbohidrogen birləşmələrindən biri olan metandır. Metananın inkişafını və istifadəsini sürətləndirmək enerji və kimya sənayesinin yaşıl və davamlı inkişafını həyata keçirmək üçün açardır. Bir yanacaq kimi birbaşa istifadəsinə əlavə olaraq, metan bir C1 resursu kimi istifadə edilə bilər, yəni bir karbon atomu olan bir molekul və metanol, formatika kimi yüksək dəyərli kimyəvi maddələr hazırlamaq üçün çevrilə bilər turşu və s. Metan su və karbon qazı yaratmaq üçün oksigendə yandırıla bilər. Yanma olmadan, yüngül şəraitdə metan molekullarının karbohidrogen bağlarını aktivləşdirmək və çevirmək mümkündürmü? Cavab bəli! Bu kataliz sahəsində "müqəddəs grail" reaksiyasıdır. "Müqəddəs Grail" ilə əlaqəli reaksiyalar çox vaxt çox çətindir, çünki çox sərt şəraitdə aparılmalı və ya yüksək sabit birləşmələrin aktivləşdirilməsi kimi kimyəvi reaksiyanın xas olan çətinliklərini dəf etməli ola bilərlər məhsul verir və aşağı seçimdir. Bu çətinliklər bu reaksiyaları həyata keçirməyi çətinləşdirir, amma uğurla əldə edilə bilsələr, elmi tədqiqat və sənaye tətbiqlərində əhəmiyyətli irəliləyişlərə səbəb olacaqdır.

1. Aşağı temperaturda metan çevrilməsində Metani aşağı temperaturda və ya hətta otaq temperaturunda ucuz oksigen olan digər faydalı kimyəvi maddələrə birbaşa çevirmək çox çətindir, niyə bu? Metan və oksigenin təbiətinə baxaq. Metanin kimyəvi quruluşu, yüksək simmetrik ortotetrajedral konfiqurasiyanı təşkil edən dörd eyni karbon-hidrogen istiqrazını (CH) ehtiva edir və hər bir CH3-H metan bağının 435 kj / mol-a qədər istiqraz enerjisinə malikdir. Metanın xüsusilə güclü bir bahar kimi ch bağını düşünə bilərik. Bu bahar çox tautdur və uzanmağa çox güc tələb edir. Kimya-da bu "qüvvə" CH bağını pozmaq üçün tələb olunan enerjidir. Bu yüksək istiqraz enerjisi metanın ch istiqrazlarını termodinamik olaraq sabit və normal şəraitdə pozmaq və ya reaksiya vermək çox çətindir. Digər tərəfdən, kimyəvi reaksiyalarda, reaktiv qruplar ümumiyyətlə qütbün qarşılıqlı əlaqəsi altında yaradılır (qütb qarşılıqlı bir molekulun bir ucu, digəri mənfi ittiham olunan və metan molekulunun qeyri-şoular təbiəti olduğu halda qarşısını alır Bu belə polarite yaratmaqdan (molekulyar konfiqurasiyaya görə, simmetriya təyyarəsi olan bir molekulun polariti yoxdur) və reaktiv qruplar verə bilməz. Buna görə metanın aktivləşdirilməsi və çevrilməsi çox çətin və ümumiyyətlə, yüksək temperatur (600-1100 ° C) və ya metanın aktivləşdirilməsində kömək etmək üçün yüksək temperatur (600-1100 ° C) və ya sərbəst radikallar kimi sərt şərtlər tələb olunur. Buna görə metan və oksigenin aşağı temperaturu aktivləşdirilməsini həyata keçirmək üçün əsas çətinlik metanın CH bağını necə aktivləşdirməkdə, yəni CH Bond-da "Bahar" nı necə uzatmaq olar. 2. Katalizatorun möcüzəsi Elm adamları bu problemin yaxşı bir həlli ilə tanış oldular və metanı aşağı temperaturda aktivləşdirməyə kömək etmək üçün bir katalizatordan istifadə etməyi seçdi (bir katalizator reaksiya əvvəl və ya sonra dəyişməyən bir kimyəvi maddəni dəyişir, lakin minimum məbləği dəyişdirərək reaksiyanı sürətləndirir baş tutacaq reaksiya üçün enjekte edilməsi lazım olan enerji). 2023-cü ildə Jurnal Təbiət Kataliz, metan oksidləri (metanol (ch3oh), formal turşusu (HC3OH) və metilen glikol (Hoch2oh) və metilen glikol (HOCH2OH), metilen glikol (HOCH2OH)) ilə birbaşa çevrilməsinə (MOS2) 25 ° C-də katalizator. 4,2% və demək olar ki, 100% C1 oksigenli bir metan çevrilməsi metan və oksigeni ətraf mühit şəraitində qiymətli C1 oksigenlesinə çevirərək əldə edildi. Bu MOS2, bu günə qədər bu günə qədər metan və oksigenin otaq temperaturun çevrilməsini həyata keçirə biləcək yeganə katalizatordur. Bu, hamısı MOS2 kənarındakı MO saytının unikal həndəsə və elektron quruluşu ilə əlaqədardır. Bu MO saytı sulu bir mühitdə oksigen istiqamətində yüksək aktivləşdirmə fəaliyyətinə malikdir, sehrli o = mo = o * növləri meydana gətirir. Bu növ, karbon hidrogen bağını metanın CH-nin CH bağının aktivləşdirmə enerjisini pozmaq və azaltmaq, beləliklə metanın reaktivliyini artırır və beləliklə metan və oksigenin aşağı temperaturlu aktivləşdirilməsini həyata keçirir. Bu kəşf gələcək enerji istifadəsi və ətraf mühitin qorunması, habelə katalizatorların və köməkçilərin inanılmaz rolunu daha da dərin bir anlayış vermək üçün daha çox imkanlar əldə edəcəkdir.
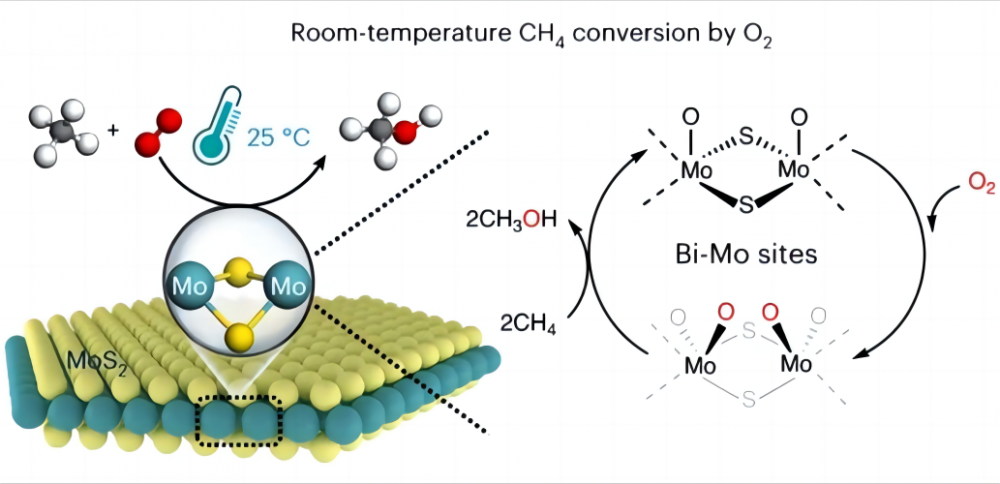
Metanın aşağı temperaturlu aktivləşdirilməsinin 3. -nik strateji əhəmiyyəti Otaq temperaturunda metan və oksigenin birbaşa katalitik çevrilməsini həyata keçirmək və təbii qazda digər faydalı kimyəvi maddələrə, tullantıların istifadəsini azaltmaq və ətraf mühitin istifadəsini daha yaxşı qorumaq və enerjinin davamlı inkişafını həyata keçirə bilər . İkincisi, istixana qazı olaraq, metan qlobal istiləşməyə verdiyi töhfədə yalnız karbon qazı üçün ikinci yerdədir. Metan digər maddələrə çevrilə bilərsə, bu, hava çirkləndiricilərinin (məsələn, karbon oksidləri, azot oksidləri, karbohidrogenlər və eter birləşmələri) və qlobal istiləşmənin təzyiqini azaltmağımıza kömək edə bilər.




